一、为何选择环状RNA?超越线性RNA的优势
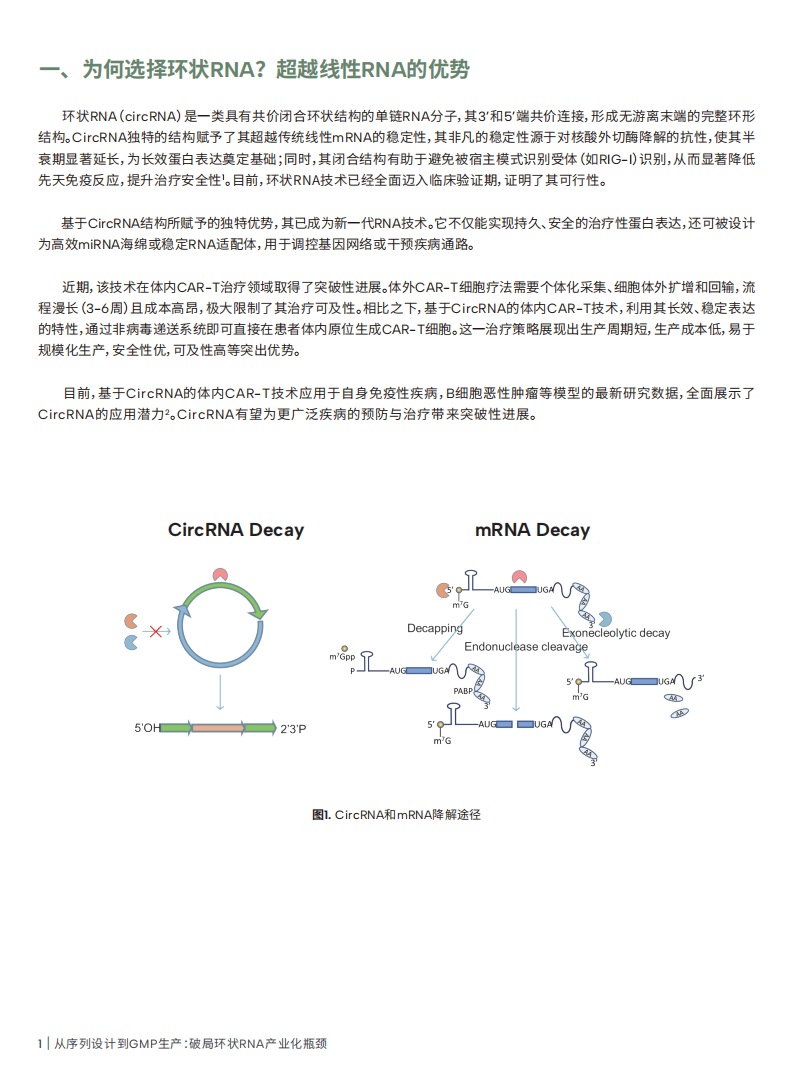
环状RNA(circRNA)是一类具有共价闭合环状结构的单链RNA分子,其3‘和5’端共价连接,形成无游离末端的完整环形结构。CircRNA独特的结构赋予了其超越传统线性mRNA的稳定性,其非凡的稳定性源于对核酸外切酶降解的抗性,使其半衰期显著延长,为长效蛋白表达奠定基础;同时,其闭合结构有助于避免被宿主模式识别受体(如RIG-1)识别,从而显著降低先天免疫反应,提升治疗安全性。目前,环状RNA技术已经全面迈入临床验证期,证明了其可行性。
基于CircRNA结构所赋予的独特优势,其已成为新一代RNA技术。它不仅能实现持久、安全的治疗性蛋白表达,还可被设计为高效miRNA海绵或稳定RNA适配体,用于调控基因网络或干预疾病通路。
近期,该技术在体内CAR-T治疗领域取得了突破性进展。体外CAR-T细胞疗法需要个体化采集、细胞体外扩增和回输,流程漫长(3-6周)且成本高昂,极大限制了其治疗可及性。相比之下,基于CircRNA的体内CAR-T技术,利用其长效、稳定表达的特性,通过非病毒递送系统即可直接在患者体内原位生成CAR-T细胞。这一治疗策略展现出生产周期短,生产成本低,易于规模化生产,安全性优,可及性高等突出优势。
目前,基于CircRNA的体内CAR-T技术应用于自身免疫性疾病,B细胞恶性肿瘤等模型的最新研究数据,全面展示了CircRNA的应用潜力²。CircRNA有望为更广泛疾病的预防与治疗带来突破性进展。
二、CircRNA面临的双重设计挑战:体外环化策略与蛋白翻译效率
1.CircRNA体外环化策略:挑战与ProBio解决方案
目前,为满足生物医学研究和临床应用的需求,CircRNA的体外环化技术已发展出多种方法,主要包括酶法连接和核酶剪接法两大技术路线。
酶法连接
该方法是一种经典的体外环化方法。通过DNA或RNA”夹板”(splint)序列引导,利用T4 DNA连接酶或T4 RNA连接酶催化线性RNA前体的5′-磷酸末端和3′-羟基末端形成磷酸二酯键3。然而,其连接效率极易受RNA二级结构影响,导致长链RNA分子(>1000 nt)的环化效率通常较低,且易产生分子间连接的副产物,因此更适用于短链RNA的环化。
核酶剪接法
该方法(l型及II型内含子系统)模拟了天然的自剪接机制。通过核酶的特殊向导序列,使剪接位点在空间上相互靠近,实现精准环化。相对于酶法连接,核酶剪接法无需蛋白质酶的参与,可显著降低CircRNA生产成本。同时,该方法能够实现长链RNA的高效环化。因此,目前核酶剪接法已成为优选的CircRNA体外合成策略。
由于核酶自身的折叠构象容易受到目的环化序列干扰,导致环化效率不稳定,通用的优化策略为在剪接位点与目标环化序列之间插入间隔和底物增强序列以消除干扰4,从而实现环化效率提升,但这种设计方式会引入外源性的核酸序列,容易引发宿主先天免疫反应56。一种改良的核酶剪接法”无痕环化策略”通过将环化位点设计在目标环化序列中,从而完全消除外源性疤痕序列,但这种环化策略由于核酶缺乏间隔序列和底物增强序列的保护,其附近复杂的局部二级结构不利于核酶的正确折叠,导致核酶失去剪接活性,因此其环化率往往不稳定’。针对上述技术瓶颈,ProBio体外环化平台构建了一个由自有环化专利技术驱动的全面的环化体系,提供三种体外环化
解决方案,可精准匹配不同阶段与场景的应用需求。有痕环化方案:基于成熟的自剪接自环化机制,通过引入底物增强序列提高环化率与稳健性。ProBio通过序列优化尽可能缩短底物增强序列的长度(可缩短至<10 nt),降低或消除其作为“疤痕”序列所引发的宿主免疫反应5。
在有痕方案的基础上,ProBio还提供两种无疤痕环化方案:
定制化无痕方案:该方法是一种完全定制化的环化路线,通过整合序列优化与智能位点筛选策略,可为任何目标序列(包括非编码RNA)设计无疤痕环化方案,尤其适合在早期研发阶段有特殊序列需求的研究(例如非编码CircRNA制备),但其环化效率需经湿实验验证,对过短或过长的序列存在适应性挑战。ProBio平台通过自由能计算与动态折叠模拟,预测并规避不利于环化的局部结构,同时提供多位点筛选服务,通过小规模实验确定最优环化条件,从而将单轮成功率提升至50%以上。
即插即用无痕方案:采用预筛选的环化元件与固定位点,具有“即插即用”特性,无需定制设计即可实现500-3000 nt蛋白表达型CircRNA的高效、无疤痕环化,并支持并行构建不同IRES和不同密码子优化的circRNA库,极大缩短筛选周期。
总体而言,ProBio的体外环化设计平台兼顾了通用性、稳健性与灵活性,用户可根据序列长度、应用场景(编码/非编码)以及对免疫原性的要求进行选择。
2.circRNA蛋白表达:挑战与ProBio解决方案
除环化策略外,如何提高CircRNA的蛋白表达效率也是CircRNA药物开发中所面临的重要挑战之一。与依赖于5’帽结构的mRNA不同,CircRNA则是通过功能元件IRES启动翻译。因此,其表达性能主要由IRES的性能与编码序列的密码子优化(常用CAI衡量)共同决定。然而简单地组合一个高性能的IRES和一个高CAI值的编码区并非最优,甚至可能不利于表达。IRES作为circRNA启动蛋白质翻译的关键元件,其功能高度依赖于形成正确的折叠构象,以有效招募核糖体启动翻译;但这种功能性构象易受编码区序列的干扰,破坏其结构完整性,反而导致翻译起始效率下降。
因此,理想的CircRNA设计需要对IRES构象稳定性与编码区翻译延伸速率进行协同优化。ProBio基于大量分子设计验证建立的CircRNA设计体系,可通过平衡两者在序列层面的制约关系,从而系统性显著提升CircRNA的整体表达性能8。
3.环状RNA生产与分析检测:挑战与ProBio解决方案
高效环化与高纯度产物的协同优化,是CircRNA在生产工艺方面的核心挑战。整个工艺流程涵盖体外转录(IVT)、环化、模板DNA去除、去磷酸化、纯化及除菌过滤等关键步骤。其中,环化反应的调控尤为关键。
环化效率受温度、反应液组分和时间等参数影响。环化反应过程中会伴随内含子核酶片段作为副产物产生。此外,环化效率不足会导致线性RNA前体(preRNA)残留,环化反应过度则引发CircRNA断裂,产生开环RNA(nicked RNA),开环RNA因其长度、序列与结构与CircRNA高度相似而极难实现分离和去除。
CircRNA制备过程中残留的RNA污染物是引发免疫反应的主要因素。线性RNA杂质中可能包含未去除的5′三磷酸基团,从而激活I型免疫反应,而开环RNA亦会被Toll样受体识别从而激活免疫反应。因此,CircRNA的成环过程中所产生的杂质和副产物(线性前体、开环RNA、核酶片段等)给纯化工艺及纯度分析方法带来了双重挑战。

本文来自知之小站
报告已上传百度网盘群,限时15元即可入群及获得1年期更新
(如无法加入或其他事宜可联系zzxz_88@163.com)